Das Periodensystem ist ein wichtiges Hilfsmittel in der Chemie. Wie es aufgebaut ist und wie du es auf einfache Weise verstehen kannst, erklären wir dir hier oder im Video .
Das Periodensystem der Elemente kannst du dir hier als Datei herunterladen und ausdrucken.
Inhaltsübersicht
Was ist das Periodensystem?
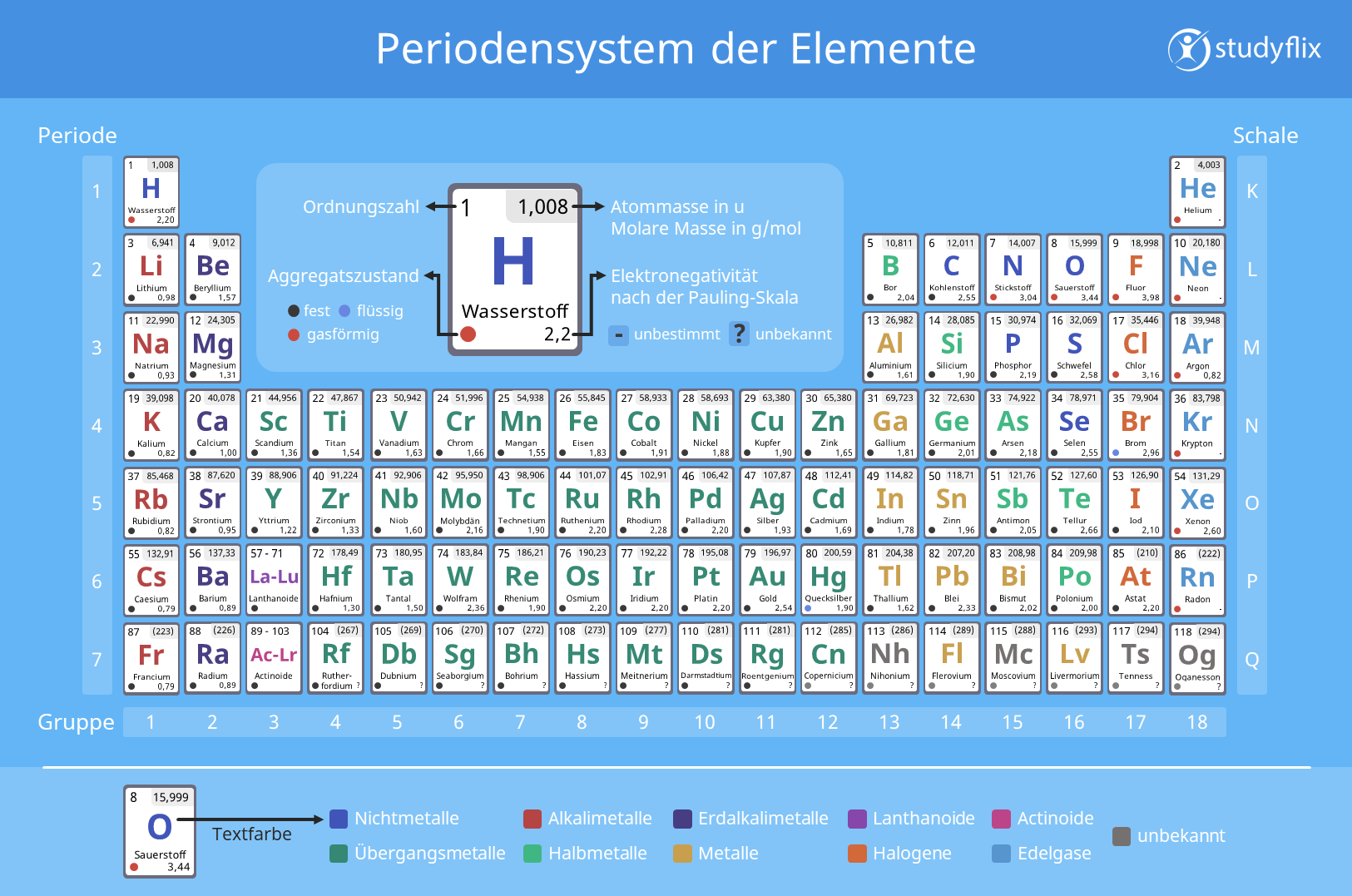
Im Periodensystem sind alle 118 chemischen Elemente in Form einer Tabelle geordnet. Deswegen nennst du es auch Periodensystem der Elemente (PSE ). Ein Element ist ein Stoff, der stets aus gleichen Atomen zusammengesetzt ist. Beispiele für chemische Elemente sind:
- Aluminium (Al)
- Sauerstoff (O)
Die Reihenfolge der Elemente im Periodensystem ist durch eine bestimmte Zahl festgelegt. Die Zahl ordnet die Elemente, deshalb heißt sie Ordnungszahl. Somit bestimmt sie die Position eines Elements.
Das Periodensystem beginnt links oben (Wasserstoff). In jeder Zeile zählst du die Ordnungszahl du von links nach rechts immer eins höher. Wenn du am Ende einer Zeile angelangt bist, zählst du links in der nächsten Zeile darunter weiter. Du liest das Periodensystem wie einzelne Zeilen in einem Buch.
Periodensystem Erklärung Aufbau
Der Aufbau des Periodensystems hat vier wichtige Merkmale:
- Ein chemisches Element ist durch seine Ordnungszahl gekennzeichnet.
- Chemische Elemente sind in Zeilen und Spalten einsortiert.
- Die Zeilen nennst du auch Perioden.
- In den Spalten sind die Elemente zu Gruppen zusammengefasst.
Die einzelnen Merkmale erklären wir dir im Laufe des Artikels.
Das Periodensystem folgt also einem logischen Aufbau. Die ersten Chemiker, die das erkannten, waren Lothar Meyer und Dmitri Mendelejew. Sie legten im 19. Jahrhundert eine wichtige Grundlage für das heute noch gültige Periodensystem.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
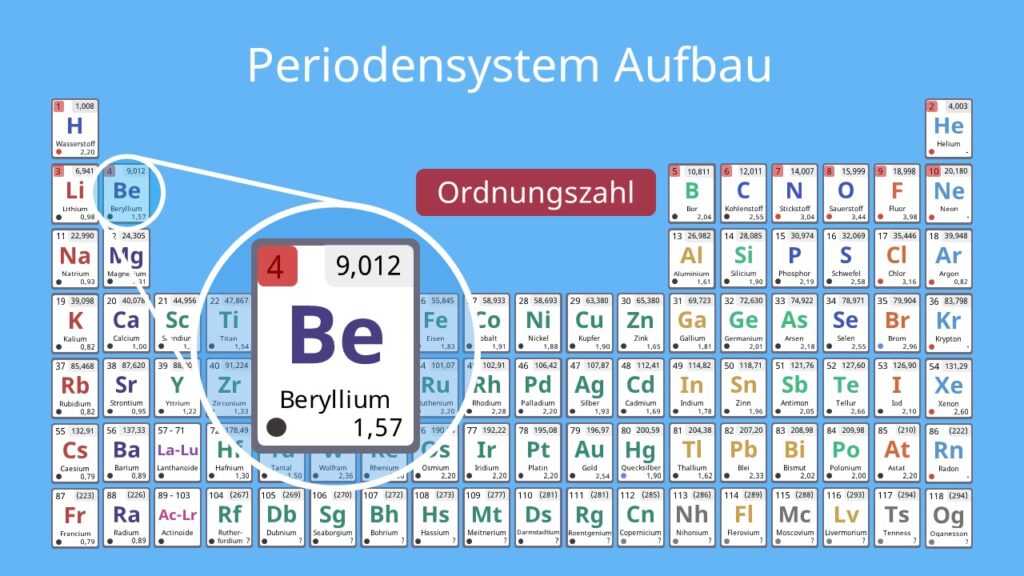
Ordnungszahl
Die Ordnungszahl gibt dir Informationen über den Aufbau eines Atoms. Denn sie ist gleich der Anzahl der Protonen im Atomkern. Deswegen nennst du die Ordnungszahl auch Kernladungszahl.
Ordnungszahl = Anzahl der Protonen im Atomkern
Zusätzlich ist sie gleich der Anzahl der Elektronen , die sich in der Elektronenhülle um den Kern bewegen. Schau dir das am Beispiel des Wasserstoffatoms an.
- Das Element Wasserstoff hat die Ordnungszahl 1.
- Deshalb befindet sich im Atomkern ein positiv geladenes Proton.
- Weiterhin bewegt sich ein negativ geladenes Elektron um den Kern.
Daraus folgt, dass die Elemente im Periodensystem immer elektrisch neutral sind. Denn die gleiche Anzahl positiver und negativer Ladungen hebt sich auf.
Die Größe der Atome steigt mit höherer Ordnungszahl. Das kannst du dir mit folgender Aussage einfacher merken.
Merke: Im Periodensystem stehen die kleinen Atome am Anfang und die großen am Ende.
Perioden und Gruppen
Das Periodensystem besteht aus Perioden und Gruppen, in welche die Elemente eingeordnet sind. Die Zeilen sind die Perioden. Zusätzlich zeigen die Spalten die verschiedenen Gruppen.
Perioden
Du zählst die Perioden im PSE von oben nach unten. Die Perioden stehen in einem Zusammenhang mit den Elektronen.
Die Elektronen in der Hülle bewegen sich auf sogenannten Schalen um den Kern. Je mehr Elektronen ein Atom hat, desto mehr Schalen braucht es, um die Elektronen zu verteilen. Du kannst dir merken, dass die Periode, in der ein Element steht, der Anzahl der Schalen entspricht. Das zeigen wir dir am Beispiel des Elements Lithium (Li).
- Lithium hat die Ordnungszahl 3. Das siehst du beispielsweise daran, dass es drei Protonen im Kern hat.
- Du findest Lithium in der zweiten Periode. Wie du siehst, hat sein Atom neben dem Atomkern zwei Schalen.
Die ersten beiden Elektronen befinden sich in der ersten, inneren Schale. Jedoch passt das dritte Elektron nicht mehr in die erste Schale, weshalb eine zweite Schale notwendig ist.
In unserem Beitrag zum Schalenmodell findest du genauere Informationen. Beispielsweise wie viele Elektronen in die jeweiligen Schalen hineinpassen.
Gruppen
Im Periodensystem sind die verschiedenen Gruppen in den Spalten geordnet. Chemische Elemente, die in einer Gruppe stehen, haben sehr oft ähnliche chemische Eigenschaften.
Du unterscheidest im Periodensystem allgemein zwischen:
- Hauptgruppen
- Nebengruppen
Im Periodensystem gibt es acht Hauptgruppen und zehn Nebengruppen.
Die Hauptgruppen haben teilweise bestimmte Namen. Dabei stammen die Namen aus den Eigenschaften ihrer jeweiligen Elemente.
Die Halogene (Gruppe 17: F, Cl, Br, I) beispielsweise bilden mit Metallen der ersten und zweiten Hauptgruppe gerne ionische Verbindungen, also Salze . Aus dem Griechischen übersetzt bedeutet Halogene „Salzbildner“.
Elementkarte
Wie du siehst, sind die Elemente im Periodensystem in Kästchen eingeteilt. Das nennst du auch Elementkarte. Jedes Element besitzt seine eigene Elementkarte, welche die Informationen zu den Eigenschaften beinhaltet. Für das Element Wasserstoff erklären wir dir, was du beispielsweise auf einer Elementkarte finden kannst.
Für Wasserstoff findest du dort folgende Informationen:
- links oben: Ordnungszahl (1)
- rechts oben: Atommasse (1.008 u)
- Mitte: Elementsymbol mit Elementname
Periodensystem zum Ausdrucken
Wenn du das Periodensystem immer griffbereit haben möchtest, kannst du es hier als Datei herunterladen und ausdrucken.
Periodensystem Erklärung — häufigste Fragen
(ausklappen)
Periodensystem Erklärung — häufigste Fragen
(ausklappen)-
Wie finde ich im Periodensystem raus, wie viele Außenelektronen ein Element hat?Bei Hauptgruppenelementen liest du die Anzahl der Außenelektronen an der Hauptgruppe ab. In den Gruppen 1, 2 sowie 13–18 gilt: Außenelektronen = 1, 2, 3, 4, 5, 6, 7, 8 (Helium hat 2). Zum Beispiel hat Chlor (Gruppe 17) 7 Außenelektronen.
-
Wie kann ich aus der Stellung im Periodensystem vorhersagen, ob ein Element eher Metall oder Nichtmetall ist?Du erkennst Metalle meist links und in der Mitte, Nichtmetalle rechts oben im Periodensystem. Dazwischen liegt eine „Treppenlinie“ (z. B. bei B, Si, Ge), an der die Halbmetalle stehen. Deshalb ist Natrium links klar metallisch, während Sauerstoff rechts oben ein Nichtmetall ist.
-
Was ist der Unterschied zwischen Atommasse im Periodensystem und Massenzahl von einem Atom?Die Atommasse im Periodensystem ist ein Durchschnittswert über alle Isotope eines Elements. Die Massenzahl gehört zu einem einzelnen Atom und ist
 . Deshalb kann Chlor eine Atommasse von etwa 35,45 u haben, aber einzelne Chlor-Atome haben Massenzahl 35 oder 37.
. Deshalb kann Chlor eine Atommasse von etwa 35,45 u haben, aber einzelne Chlor-Atome haben Massenzahl 35 oder 37.
-
Welche typischen Fehler passieren beim Ablesen von Gruppen und Perioden im Periodensystem?Häufig werden Zeilen und Spalten verwechselt: Perioden sind waagerecht, Gruppen senkrecht. Ein weiterer Fehler ist, die Außenelektronen-Regel auf Übergangsmetalle anzuwenden, obwohl sie für Hauptgruppen gedacht ist. Außerdem wird Wasserstoff manchmal falsch als „typisches Alkalimetall“ eingeordnet, obwohl er viele Sonderfälle hat.
-
Wie erkenne ich im Periodensystem die Übergangsmetalle und warum verhalten die sich oft anders als Hauptgruppenelemente?Übergangsmetalle stehen im Block in der Mitte des Periodensystems (meist Gruppen 3–12), also zwischen den Hauptgruppen links und rechts. Sie verhalten sich oft anders, weil bei ihnen d-Elektronen mitbeteiligt sind, nicht nur Außenelektronen. Dadurch haben sie häufig mehrere Oxidationszahlen und bilden oft farbige Verbindungen.
Periodensystem Erklärung im Detail
Du kennst nun die Grundlagen des Periodensystems und weißt, welche Informationen der chemischen Elemente du daraus ablesen kannst. Wenn du mehr über das Periodensystem allgemein und seine Trends wissen musst, schau dir unbedingt unser ausführliches Video dazu an!