Osmose (Wiederholung)
Unter Osmose (griechisch. osmos = Schub, Antrieb) kannst du die Diffusion eines Lösungsmitteln durch eine semi- oder selektiv permeable Membran verstehen. Sie ist im Fall der Osmose nur für das Lösungsmittel (in der Regel Wasser) und nicht für die gelösten Stoffe durchlässig.
Wasser diffundiert aus dem Kompartiment (Raum), an dem es höher konzentriert vorliegt (geringere Teilchenkonzentration), in das Kompartiment, in dem seine Konzentration geringer ist (höhere Teilchenkonzentration). Die Bewegung läuft so lange ab, bis die Stoffkonzentrationen auf beiden Seiten ausgeglichen sind.
Osmose findet Anwendung in der Aufbereitung von Trinkwasser (Umkehrosmose), in Osmosekraftwerken, in der Dialyse zur Blutreinigung oder bei der Lebensmittelkonservierung. Sie ist lebenswichtig für uns Menschen, denn sie findet in unserem Körper in jeder einzelnen Zelle als Transportprozess statt.
Osmose in pflanzlichen und tierischen Zellen
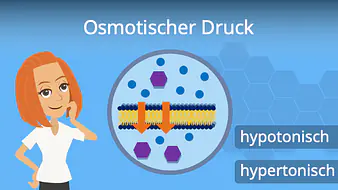
Wie du bereits gelernt hast, findet Osmose als Transportprozess von Wasser zwischen Zellen statt. Generell gibt es drei Begriffe, um die Konzentrationen von Stoffen, die durch Membranen getrennt sind, zu beschreiben: hypertonisch, isotonisch und hypotonisch.
Eine hypertonische (hyper = über, tonus = Spannung) Lösung besitzt eine höhere Konzentration an gelösten Stoffen als die Vergleichslösung. Bei isotonischen (iso = gleich) Verhältnissen sind auf beiden Seiten gleiche Konzentrationen gelöster Stoffe zu finden. Eine hypotone (hypo = unter) Lösung besitzt eine niedrigere Konzentration an gelösten Stoffen als die Vergleichslösung.
Du kannst dir folgenden Zusammenhang merken: Wasser bewegt sich immer von einer hypotonischen Lösung zu einer hypertonischen Lösung.
Natürlich findet immer ein Hin- und Rückfluss statt. Hier ist die Tendenz in eine Richtung entscheidend, also in welches Kompartiment das meiste Wasser zum Konzentrationsausgleich strömt.
Die größten Unterschiede zwischen tierischen und pflanzlichen Zellen sind, dass Pflanzenzellen zusätzlich zur Zellmembran eine Zellwand und eine Vakuole besitzen.
Studyflix vernetzt: Hier ein Video aus einem anderen Bereich
Tierische Zellen
Wir behandeln als Beispiel für tierische Zellen rote Blutzellen (= Blutkörperchen, Erythrozyten). Sie befinden sich normalerweise im Blutplasma. Darunter kannst du dir eine wässrige Lösung vorstellen, die unter anderem Salze und Proteine enthält.
Im Normalzustand besitzen rote Blutzellen die Form einer Scheibe (=bikonkav). Verdünnt man jetzt die Bluttropfen mit reinem Wasser, schwellen die Zellen an und platzen. Das reine Wasser ist also hypoton im Vergleich zum hypertonen Medium im Inneren der roten Blutzellen. Die Plasmamembran kann dem Druck des Wassereinstroms nicht standhalten und das führt zum Platzen der Zellen.
Wird im umgekehrten Fall eine relativ konzentrierte Salzlösung dem Blut zugefügt, ist nun das Zellplasma der Blutzellen hypoton im Vergleich zum Außenmedium. Das hat zur Folge, dass Wasser per Osmose austritt und die Blutzellen eine faltige Form (Stechapfelform) besitzen. Diese sind nun nicht mehr in der Lage, Sauerstoff zu transportieren, was gravierende Folgen hat. Deshalb muss beim Kochen besonders bei kleinen Kindern aufgepasst werden, dass Zucker und Salz nicht vertauscht werden.
Pflanzenzellen
Betrachten wir jetzt als Beispiel für die Pflanzenzellen Salat. Wenn wir welken Salat in destilliertes Wasser geben, kommen dessen Zellen im Gegensatz zu den Blutzellen nicht zum Platzen. Er wird stattdessen wieder knackig. Das liegt an der robusten Zellwand. Sie sorgt dafür, dass nur eine bestimmte Menge an Wasser in die Zellen – genauer gesagt in die Vakuolen – aufgenommen werden kann. Die Vakuole übt dadurch einen starken Druck auf die Zellwand aus. Du kannst dir das wie die Luft innerhalb eines Ballons vorstellen, die gegen die Ballonwand drückt.
Die Zellwand baut beim Wassereinstrom einen Druck auf – den Tugor. Er kann in der Zelle bis zu 7 bar betragen (Zum Vergleich: das ist dreimal mehr als bei einem Autoreifen.). Diese „pralle“ Zelle kannst du auch als voll turgeszent und den Vorgang als Deplasmolyse bezeichnen.
Legen wir jetzt das Salatblatt in eine konzentrierte Salzlösung, so kommt es zu einem Wasserausstrom aus der Vakuole und der Tugordruck nimmt ab. Der Zellkörper (Protoplast ) löst sich von der Zellwand. Diesen Vorgang kannst du auch als Plasmolyse bezeichnen.
Für Pflanzen ist der Wassertransport von der Wurzel enorm wichtig. Hier wird Wasser passiv über die Wurzel per Osmose aufgenommen. In biologischen Systemen spielt oft der Begriff Wasserpotential eine Rolle, wenn es um die Beschreibung des Wasserhaushaltes geht. Es beschreibt die Verfügbarkeit von Wasser in einem System wie der Luft oder dem Boden und setzt sich aus dem osmotischen Druck – also der Anzahl der gelösten Teilchen – und dem Turgordruck zusammen. Wichtig: Das Wasser fließt immer vom Ort des höheren Wasserpotentials zum Ort des niedrigeren Wasserpotentials.
Osmoregulation
Du siehst also, dass die Regulation der osmotischen Verhältnisse (= Osmoregulation) vor allem in tierischen Zellen enorm wichtig ist. Sie müssen aufpassen, dass die Zahl der gelösten Teilchen nicht zu hoch oder niedrig wird. Das hängt natürlich auch von der jeweiligen Lebensweise ab.
Viele wasserlebende Tiere müssen mit unterschiedlichen Wasser- und Salzkonzentrationen auskommen. Du kannst hier zwischen Osmokonformern und Osmoregulierern unterscheiden. Osmokonformer sind vor allem wirbellose Tiere und passen ihre Osmolarität an ihre Umgebung an.
Osmoregulierer regulieren wie ihr Name bereits vorwegnimmt, dass ihr Salzgehalt unabhängig von ihrer Umgebung fast immer konstant bleibt. Süßwasserfische beispielsweise müssen das Problem, dass ständig Wasser per Osmose einströmt, beheben. Salzwasserfische (Halophile) müssen aufpassen, dass sie nicht zu viel Wasser verlieren.
Einzeller wie das Pantoffeltierchen (Parameticum), die Alge Euglena oder Amöben haben eine besondere Lösung, ihren Wasserhaushalt zu regulieren. Sie besitzen nämlich eine kontraktile Vakuole , die sich vergrößern und verkleinern kann. Dadurch kann überschüssiges Wasser aus dem Zellplasma durch Osmose in die Vakuole einströmen und über die Zellmembran abgegeben werden.
Pflanzen besitzen zwar Anpassungen wie eine dicke Cuticula oder eingesenkte Spaltöffnungen als Schutz vor Austrocknung. Aber bis auf wenige Ausnahmen haben höhere Pflanzen keine Strukturen für Osmoregulation.
Osmose Anwendungen
Das Prinzip der Osmose wird in Technik und Medizin genutzt, erklärt aber auch viele Alltagsphänomene. In der medizinischen Dialyse werden beispielsweise mithilfe von Osmose schädliche Stoffe aus dem Blut entfernt.
Eine andere Möglichkeit der Nutzung von Osmose bietet die Umkehrosmose. Bei einer Umkehrosmose wird gemäß des Namens die Osmose umgekehrt. Mithilfe eines externen Drucks wird eine Substanz gegen ihr Konzentrationsgefälle aufkonzentriert. Diese Methode findet bei der Aufbereitung von Trinkwasser Anwendung.
Außerdem wird in Osmosekraftwerken osmotische Arbeit in Energie umgewandelt und zur Stromerzeugung genutzt.
Auch im Alltag begegnen wir dem Phänomen der Osmose häufig. Beim Kochen von Gemüse achten wir zum Beispiel darauf, dass wir Salzwasser verwenden. Dadurch wird ein Wassereinstrom in das leicht salzhaltige Gemüse vermieden, was den Geschmack beeinträchtigen würde. Auch zur Konservierung von Lebensmitteln wird häufig Zucker oder Salz (Pökeln) dazu gegeben, um das Wasser aus den Lebensmitteln „herauszuziehen“. Reife Früchte wie Kirschen platzen eben auch häufig bei Regen, da es zu einem osmotischen Wassereinstrom kommt. Die schrumpelige Haut nach dem Baden ist übrigens auch ein Ergebnis von Osmose.
Besonders tragisch sind Fälle, bei denen durch zu viel Wasseraufnahme in kurzer Zeit, wie etwa bei einem Marathon, Menschen sterben können. Durch die Wasseraufnahme sinkt die Salzkonzentration in den Zellen und Wasser strömt in die nun höher konzentrierten Hirnzellen ein. Das führt zu einer Hirnschwellung, die im schlimmsten Fall zum Tod führen kann.
Diffusion
Die Osmose ist ein Spezialfall der Diffusion und beschreibt die Bewegung von Wasser durch eine Membran. Wie sich Teilchen allgemein von Bereichen hoher zu niedriger Konzentration bewegen, erfährst du im Beitrag zur Diffusion.